
ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА ЖЕЛАТИНА
Желатин почти безвкусен и не имеет запаха. Это стекловидное, хрупкое твердое вещество слегка желтого цвета. Желатин содержит 8-13% влаги и имеет относительную плотность 1,3-1,4. Когда гранулы желатина замачиваются в холодной воде, они гидратируются в дискретные, набухшие частицы. При нагревании эти набухшие частицы растворяются, образуя раствор. Этот метод приготовления растворов желатина является предпочтительным, особенно там, где требуются высокие концентрации. Поведение растворов желатина зависит от температуры, pH, зольности, способа производства, термической истории и концентрации.Желатин растворим в водных растворах многоатомных спиртов, таких как глицерин и пропиленгликоль. Примерами высокополярных, водородно-связывающих органических растворителей, в которых растворяется желатин, являются уксусная кислота, трифторэтанол и формамид. Желатин нерастворим в менее полярных органических растворителях, таких как бензол, ацетон, первичные спирты и диметилформамид.
Желатин, хранящийся в герметичных контейнерах при комнатной температуре, остается неизменным в течение длительного времени. При нагревании сухого желатина выше 45° C на воздухе при относительно высокой влажности (выше 60% RH) он постепенно теряет способность набухать и растворяться.
Стерильные растворы желатина при хранении в холоде стабильны неограниченно долгое время; однако при повышенных температурах растворы подвержены гидролизу.
Два наиболее полезных свойства желатина — прочность геля и вязкость — постепенно ослабевают при длительном нагревании в растворе выше примерно 40 °C. Разложение может также быть вызвано экстремальными значениями pH и протеолитическими ферментами, включая те, которые могут быть результатом присутствия микроорганизмов.
Коллаген можно считать ангидридом желатина. Гидролитическое превращение коллагена в желатин дает молекулы различной массы: каждая из них является фрагментом коллагеновой цепи, от которой она была отщеплена. Таким образом, желатин не является единым химическим образованием, а представляет собой смесь фракций, состоящих исключительно из аминокислот, соединенных пептидными связями с образованием полимеров с различной молекулярной массой от 15 000 до 400 000.
Желатин, по основным элементам, состоит из 50,5% углерода, 6,8% водорода, 17% азота и 25,2% кислорода.
Поскольку он получен из коллагена, желатин правильно классифицируется как производный белок. Он дает типичные белковые реакции и гидролизуется большинством протеолитических ферментов, чтобы получить его пептидные или аминокислотные компоненты.
Различные аминокислоты, которые можно получить из некоторых желатинов путем полного гидролиза, в граммах на 100 граммов сухого желатина, перечислены в таблице.
ТАБЛИЦА 1. АМИНОКИСЛОТНЫЙ СОСТАВ ЖЕЛАТИНА
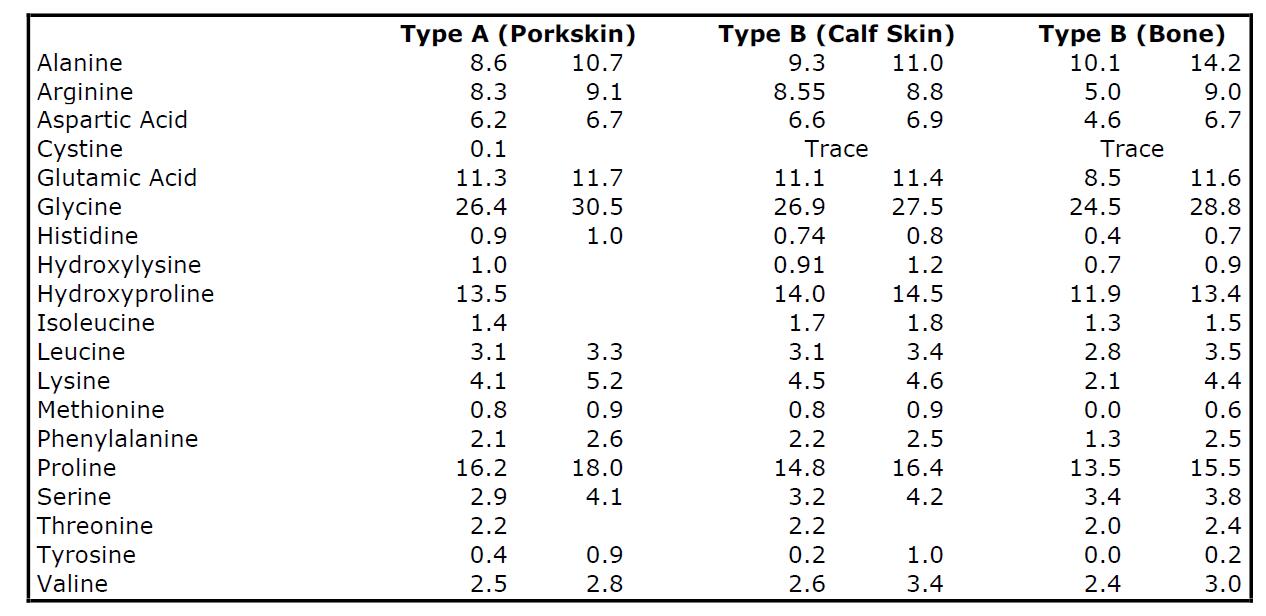
Амфотерные свойства — Желатин в растворе амфотерный, способен действовать как кислота или как основание. В кислых растворах желатин заряжен положительно и мигрирует как катион в электрическом поле. В щелочных растворах желатин заряжен отрицательно и мигрирует как анион. pH промежуточной точки, где чистый заряд равен нулю и не происходит никакого движения, известен как изоэлектрическая точка (ИЭТ). Желатин типа A имеет широкий изоэлектрический диапазон между pH 7 и 9. Тип B имеет более узкий изоэлектрический диапазон между pH 4,7 и 5,4.
Желатин в растворе, не содержащем неколлоидных ионов, кроме H+ и OH-, называется изоионным желатином. pH этого раствора называется изоионной точкой (pl). Эти растворы могут быть приготовлены с использованием ионообменных смол.
Химические производные – Желатин может быть химически обработан, чтобы вызвать значительные изменения его физических и химических свойств. Эти изменения являются результатом структурных модификаций и/или химических реакций. Типичные реакции включают ацилирование, этерификацию, дезаминирование, сшивание и полимеризацию, а также простые реакции с кислотами и основаниями.
Прочность геля – Образование термообратимых гелей в воде является одним из важнейших свойств желатина. Когда водный раствор желатина с концентрацией более примерно 0,5% охлаждается примерно до 35-40°C, он сначала увеличивает вязкость, а затем образует гель. Жесткость или прочность геля зависят от концентрации желатина, его собственной прочности, pH, температуры и наличия каких-либо добавок. Собственная прочность желатина является функцией как структуры, так и молекулярной массы.
Первым шагом в гелеобразовании является образование локально упорядоченных областей, вызванное частичным случайным возвратом (ренатурацией) желатина в коллагеноподобные спирали (коллагеновая складка). Затем по всей системе образуется непрерывная фибриллярная трехмерная сеть бахромчатых мицелл, вероятно, из-за неспецифического образования связей между более упорядоченными сегментами цепей. В образовании поперечных связей могут участвовать гидрофобные, водородные и электростатические связи. Поскольку эти связи разрушаются при нагревании, гель является термообратимым. Образование поперечных связей является самой медленной частью процесса, так что в идеальных условиях прочность геля увеличивается со временем по мере образования большего количества поперечных связей. Общий эффект заключается в зависящем от времени увеличении средней молекулярной массы и в порядке.
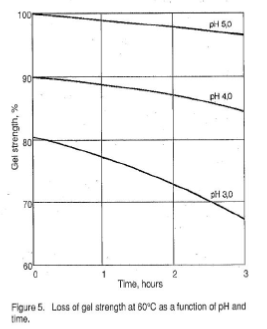
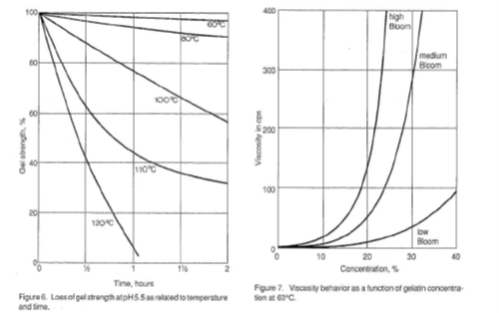
Гелеобразующее свойство желатина является важным физическим параметром качества. Измерение этого свойства очень важно как с точки зрения контроля, так и как указание количества желатина, необходимого для конкретного применения. Рисунки 2–6 иллюстрируют поведение желатиновых гелей под влиянием времени, концентрации, pH и температуры (40).
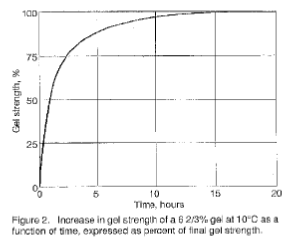
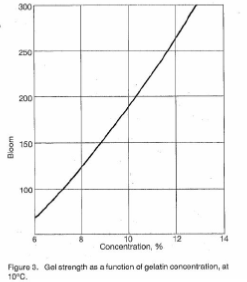
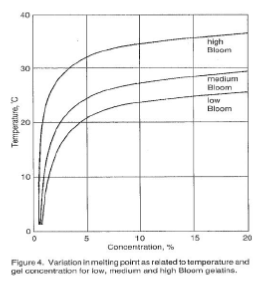
Вязкость - Установленный метод определения вязкости включает измерение времени истечения 100 мл стандартного тестового раствора из калиброванного пипеточного вискозиметра. В некоторых случаях вязкость определяется при концентрациях, при которых желатин должен использоваться.
Распределение молекулярной массы, по-видимому, играет более важную роль в влиянии на вязкость, чем на прочность геля. Некоторые желатины с более высокой прочностью геля могут иметь более низкую вязкость, чем желатины с более низкой прочностью геля.
Вязкость растворов желатина увеличивается с увеличением концентрации желатина и понижением температуры; вязкость минимальна в изоионной точке.
На рисунке 7 показано поведение вязкости для желатинов с низкой, средней и высокой степенью помутнения в зависимости от концентрации при температуре 60°C.
Защитное коллоидное действие – Желатин является типичным гидрофильным коллоидом, способным стабилизировать различные гидрофобные материалы. Эффективность желатина как защитного коллоида подтверждается его золотым числом Зигмонди, которое является самым низким среди всех коллоидов. Это свойство особенно ценно для фотографической и гальванической промышленности.
Коацервация – Явление, связанное с коллоидами, при котором диспергированные частицы отделяются от раствора, образуя вторую жидкую фазу, называется коацервацией. Обширные исследования коацервации были проведены с желатином.
Распространенным применением коацервации является использование желатина и гуммиарабика для производства маслосодержащих микрокапсул для производства безугольной бумаги (46-48). Коацервация также полезна в фотоиндустрии.
Цвет – Цвет желатина зависит от природы используемого сырья и того, представляет ли желатин первую, вторую или дальнейшую экстракцию. Желатин из свиной кожи обычно менее цветной, чем тот, что сделан из кости или шкуры. В целом, цвет не влияет на свойства желатина и не снижает его полезности.
Мутность – Мутность может быть вызвана нерастворимыми или посторонними веществами в форме эмульсий или дисперсий, которые стабилизировались благодаря защитному коллоидному действию желатина, или изоэлектрической дымкой. Эта дымка максимальна в изоэлектрической точке примерно в 2% растворах. При более высоких концентрациях или других значениях pH дымка будет заметно меньше.
Зола – Содержание золы в желатине варьируется в зависимости от типа сырья и способа обработки. Свиной желатин содержит небольшое количество хлоридов или сульфатов. Оссейновый и кожной желатины содержат в основном кальциевые соли тех кислот, которые используются при нейтрализации после золения. Ионообменная обработка может использоваться для деминерализации или удаления золы из желатина.